Enfermedad de Gaucher
Qué es la enfermedad de Gaucher?
La enfermedad de Gaucher (EG) es una enfermedad rara autosómica recesiva. Su frecuencia varía desde 1:40 000 a 1:80 000 en los nacidos vivos, alcanzando 1:800 en la población judía Ashkenazi (1).
Es una de las enfermedades lisosomales más frecuentes, causada principalmente por mutaciones del gen GBA1, que codifica la síntesis de la enzima lisosomal glucocerebrosidasa (GCasa). La deficiencia de GCasa produce la acumulación de glucosilceramida (GlcCer) en los lisosomas del sistema monocítico macrofágico de médula ósea (MO), bazo, hígado, con menor frecuencia en pulmones y en las formas neurológicas en cerebro, causando daño celular y disfunción orgánica (1).
El fenotipo más frecuente es la EG tipo I (EG1), con manifestaciones principalmente hematológicas, viscerales y esqueléticas. Las formas con afectación predominante neurológica o neuronopáticas: tipo 2 (aguda) y tipo 3 (subaguda) presentan frecuencia mucho menor (1).
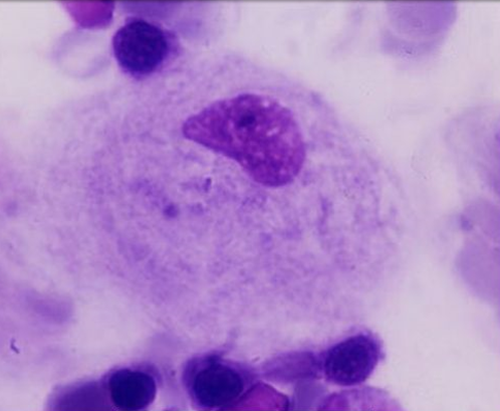
¿Cómo se diagnostica la enfermedad de Gaucher?
El diagnóstico se basa en la medición de la actividad de la enzima GCasa. La determinación, en gota seca en papel de filtro (DBS), es orientativa y sirve como tamizaje poblacional, pero debe confirmarse por medición de la actividad de GCasa en leucocitos circulantes o en cultivo de fibroblastos (1,2). El estudio molecular de la mutación del gen GBA1 ha documentado más de 400 mutaciones, algunas de ellas relacionadas con determinados fenotipos (1).
El diagnóstico de EG suele realizarse varios años luego de sus primeras manifestaciones, en promedio entre 3-4 años (rango 0,5-26 años), y habiendo consultado hasta 8 (promedio 3) médicos previamente (2,3). Los errores diagnósticos más comunes son anemia crónica, enfermedad hemato-oncológica, purpura trombótica trombocitopénica, cirrosis, esplenomegalia idiopática, necrosis ósea idiopática (2,3).
¿Cúal es el tratamiento?
Existen actualmente dos tratamientos específicos: terapia de reemplazo enzimático (TRE) y terapia de reducción de sustrato. En etapa de investigación el uso de chaperones de la enzima, como ambroxol (principalmente en formas neuronopáticas) (1). Las TRE disponibles y aprobados en la Argentina son velaglucerasa alfa e imiglucerasa. Los fármacos de reducción de sustrato (Misglustat y Eliglustat) se administran por vía oral y se basan en disminuir el exceso de GlcCer, disminuyendo su producción.
La terapia de reemplazo enzimático mejora sustancialmente la citopenia, visceromegalia, la infiltración de medula ósea, la densidad mineral ósea y disminuyen las crisis y dolor óseo y la frecuencia de lesiones óseas irreversibles. En los niños además mejora el crecimiento y el pico de masa ósea. El retraso en el inicio del tratamiento se asocia a un mayor riesgo de complicaciones, principalmente óseas y a menor eficacia del mismo (1,3-5).
Manifestaciones óseas de la enfermedad de Gaucher
Si bien la sospecha clínica de EG1 está tradicionalmente asociada a la presencia de espleno/hepatomegalia y citopenias, se ha observado que hasta 25-32% de los pacientes presentan signos y/o síntomas óseos como manifestación inicial de la enfermedad (5-7).
El 80-95% de los pacientes con EG1 (incluso los asintomáticos) tienen alguna manifestación clínica o radiológica de afectación ósea al momento del diagnóstico. Las diferentes series han documentado: infiltración de médula ósea 60-80%, deformidad de Erlenmeyer 49-63%, lesiones líticas 7-34%, infartos óseos 8-24%, necrosis ósea avascular 8-30%, osteopenia 20-49% y fracturas 11-20%. El 27-63% refiere antecedentes de dolor óseo y el 9-20% antecedentes de crisis óseas.
La patología esquelética representa uno de los aspectos más debilitantes de la enfermedad ya que algunas de sus secuelas son irreversibles. No siempre correlaciona con el compromiso visceral o hematológico (1).
La localización, extensión y severidad de las complicaciones óseas y su seguimiento se evalúan por radiología simple, resonancia magnética nuclear (RMN) de columna vertebral y fémures (análisis de la infiltración de la médula ósea), densitometría ósea y laboratorio (1,4,5).
La fisiopatología de la afectación ósea es multifactorial (1,4). La acumulación de glucocerebrósidos en médula ósea causa expansión centrífuga de la médula ósea con aumento de la presión local, alteración de la microvascularización e isquemia, causando adelgazamiento cortical, necrosis ósea avascular, infartos y crisis óseas. Promueve el reclutamiento de macrófagos proinflamatorios en el microambiente óseo con secreción de citoquinas, chemoquinas y factores inflamatorios. La interrelación entre el sistema inmune y las células óseas, con desbalance entre la resorción y formación ósea influyen en el desarrollo de osteopenia, osteoporosis y fracturas. También presentan alta prevalencia de deficiencia vitamina D.
Algoritmo diagnóstico para detección precoz de enfermedad de Gaucher
El diagnóstico temprano de enfermedad de Gaucher y el tratamiento oportuno disminuyen el riesgo de desarrollar complicaciones asociadas a la EG (1-3).
Los algoritmos de rastreo se han basado se han basado en la esplenomegalia, hepatomegalia y citopenias dichas manifestaciones (2). Considerando la alta prevalencia de signos y síntomas óseos al diagnóstico y como primera manifestación, se ha implementado un proyecto para la detección precoz de EG (BIG: Bone Involvement Gaucher Disease) que incluye un programa educativo y un algoritmo diagnóstico (6,7). Los signos y síntomas óseos que deben alertar al profesional de la salud incluyen: osteomielitis, enfermedad de Perthes, crisis óseas, artroplastia de cadera (no asociada a artrosis traumatismo o artritis reumatoidea), fracturas recurrentes, dolores óseos y necrosis ósea avascular sin causas identificadas. Ante la presencia de alguno de estas manifestaciones, luego de obtención de consentimiento informado, se realiza medición de la actividad de GCasa en gotas de sangre seca en papel de filtro (DBS). Si el resultado muestra actividad enzimática reducida, se solicita la medición en leucocitos circulantes. La actividad normal de GCasa descarta EG.
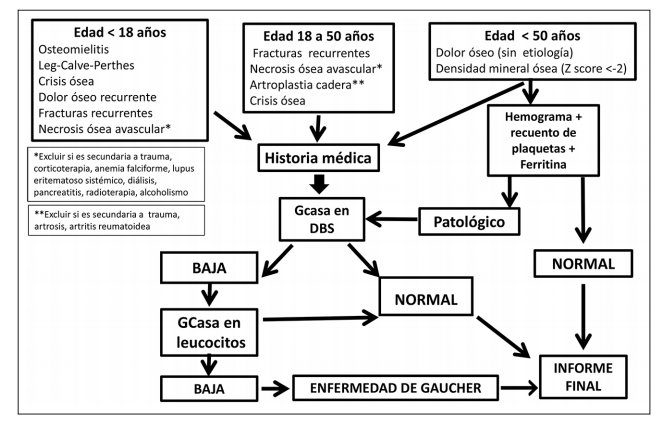
Oliveri B, González DC, Rozenfeld P, Ferrari E, Gutiérrez G. Diagnóstico temprano de enfermedad de Gaucher mediante detección de manifestaciones óseas. Medicina (Buenos Aires) 2020, 80:487-494
Conclusión
Es fundamental la difusión del conocimiento de EG para su detección y tratamiento temprano para mejor evolución y calidad de vida y evitar complicaciones irreversibles.
Referencias bibliográficas
- Stirnemann J, Belmatoug N, Camou F, et al. A review of Gaucher disease pathophysiology, clinical presentation and treatments. Int J Mol Sci 2017; 18: E441.
- Mistry PK, Cappellini MD, Lukina E, et al. A reappraisal of Gaucher disease -diagnosis and disease management algorithms. Am J Hematol 2011; 86: 110-115.
- Thomas AS, Mehta AB, Hughes DA. Diagnosing Gaucher disease: an on-going need for increased awareness amongst haematologists. Blood Cells Mol Dis 2013; 50: 212-217
- Hughes D, Mikosch P, Belmatoug N et al: Gaucher disease in bone: from pathophysiology to practice. J Bone Min Res 2019 DOI 10.1002/jbmr37345
- Oliveri B, González D, Quiroga, F, Silva C, Rozenfeld P. A comprehensive study of bone manifestations in adult Gaucher Disease type 1 patients in Argentina. Calcif Tissue Int 2019; 104: 1-8
- Oliveri B, González DC, Rozenfeld P, Ferrari E, Gutiérrez G. Diagnóstico temprano de enfermedad de Gaucher mediante detección de manifestaciones óseas. Medicina (Buenos Aires) 2020, 80:487-494
- Oliveri B, Gonzalez D C , Ferrari: Bone symptoms can be an early manifestation of Gaucher disease implications for diagnosis, Endocrine and Metabolic Science 2020, doi: https://doi.org/10.1016/j.endmts.2020.100050